


藥物的低選擇性往往會帶來不必要的毒副作用。要想徹底克服這一問題,需要在分子層面實現對藥物活性的精準調控,從根本上消除藥物本身帶來的不良影響。隨著機械力化學(Mechanochemistry)領域的興起和快速發展,機械力逐漸展現出其在分子水平調控化合物化學性質的優勢和潛力,為實現藥物活性的精確調控提供了可能。
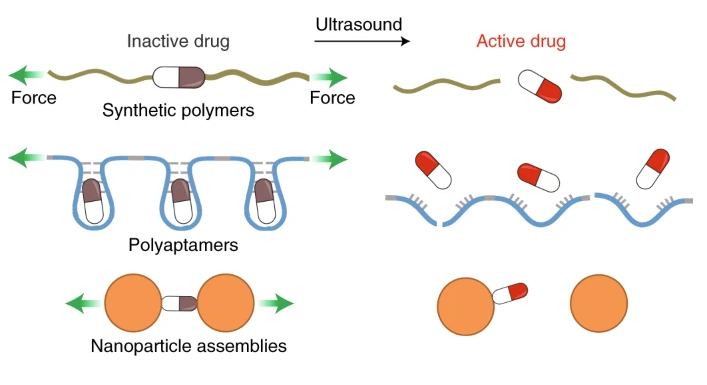
在此項成果中,研究人員利用超聲機械力化學,通過三種不同策略分別實現了對弱共價鍵或非共價鍵的選擇性斷裂,首次實現了對聚合物或納米結構中小分子化療藥物的精準激活。第一種策略是依靠以抗癌藥喜樹堿(CPT)為中心的二硫化聚合物,超聲機械力的施加可選擇性切斷二硫鍵,使其轉化為硫醇并促進分子內5-exo-trig環化作用,從而釋放并活化喜樹堿分子。第二種策略依賴于RNA適配體與其靶分子的結合作用。其中,實驗合成的高分子量多適體可與多個抗生素新霉素B(Neomycin B)或巴龍霉素(Paromomycin)結合并抑制其活性。超聲機械力的施加可破壞結構中的非共價鍵作用,進一步導致RNA主鏈的部分共價鍵斷裂,從而釋放并激活藥物分子。第三種方法則是基于對機械力敏感的前藥組裝體中萬古霉素(Vancomycin)與其短肽靶序列之間的超分子結合作用。超聲機械力的施加可選擇性破壞結構(聚合物-納米顆粒或納米顆粒-納米顆粒)中的多氫鍵作用,從而在分子層面激活抗生素藥物分子的活性。
該項成果是利用機械力在分子層面實現藥物活性精準調控的首次報道,提供了一種極限精準的治療策略。值得一提的是,英國利物浦大學的Roman Boulatov教授在同期News & Views專欄對該工作進行了亮點評述,其中他提到:“These results offer a promising approach that can be tailored to diverse molecular structures of modern pharmaceuticals”。該項研究不僅有助于發展基于超聲力化學的藥物活化治療新策略,為解決當前醫學領域的重要難題提供新思路,更有利于加深人們對機械力在微觀生命活動中扮演重要角色的進一步理解。
參考資料
[1] 廈門大學,Nature Chemistry | 藥學院霍帥東教授合作發表機械力選擇性激活藥物的重要進展,https://pharm.xmu.edu.cn/2021/0131/c19556a426413/page.htm
[2] 文章鏈接:https://www.nature.com/articles/s41557-020-00624-8
[3] 評述鏈接:https://www.nature.com/articles/s41557-020-00623-9
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn