

吲哚骨架廣泛存在于生物活性結構和藥物分子中,由于吲哚中吡咯側具有較高的親核性,化學家們已成功地在吲哚的C2或C3位實現了選擇性的C-H官能團化。近年來,利用吲哚氮原子上的可脫除導向基團(DG),在C6或C7位引入官能團的方法也得到了發展。而直接構建C4位官能團化的吲哚是一個尚未解決的問題,引起了人們的廣泛關注(圖1a)。

圖1. 4-氨基吲哚的合成方法及其生物活性(圖片來源:J. Am. Chem. Soc.)
4-氨基吲哚是一種具有廣泛生物活性的分子骨架,其中4-哌嗪吲哚可作為G蛋白受體(GPCR)靶點的分子砌塊。GPCR靶標已成為制藥業的一個重要研究熱點,在過去的10年中已經推出了60多種新的GPCR藥物 (圖1b)。盡管具有4-氨基吲哚骨架的化合物普遍具有生物活性,但其合成方法較少。因此,開發一系列的C-H胺化反應,從簡單的原料中一步構建4-氨基吲哚骨架是非常有價值的。
2009年,M. Lautens等人使用降冰片二烯(NBD),并通過逆Diels-alder策略成功地獲得了C2,C3-非取代的吲哚。當鄰碘苯胺氮上的保護基為吸電子基時,反應選擇性地向Buchwald偶聯反應進行。當添加鹵化烷烴時,仍然不能改變反應方向。2000年,M. Lautens首次使用膦配體來拓寬Pd/NBE的化學兼容性,并建立了Catellani-Lautens反應體系。2013年,董廣彬首次利用親電胺化試劑實現了鄰位胺化反應,為設計和構建4-氨基吲哚提供了有力的工具。2016年,余金權首次開發了一種吡啶衍生物作為引導基團的間位C-H胺化反應,可用于合成3-氟-5-嗎啉苯胺。在過去的20年中,M. Lautens等研究小組開發了一系列的分子內Pd/NBE反應來構建各種雜環或非雜環骨架。然而,通過多米諾反應一步構建C4官能團化吲哚骨架的研究至今未見報道。近日,蘭州大學梁永民教授課題組通過Catellani和逆Diels-Alder策略高效合成了C4-氨基吲哚,文章發表在J. Am. Chem. Soc.上。
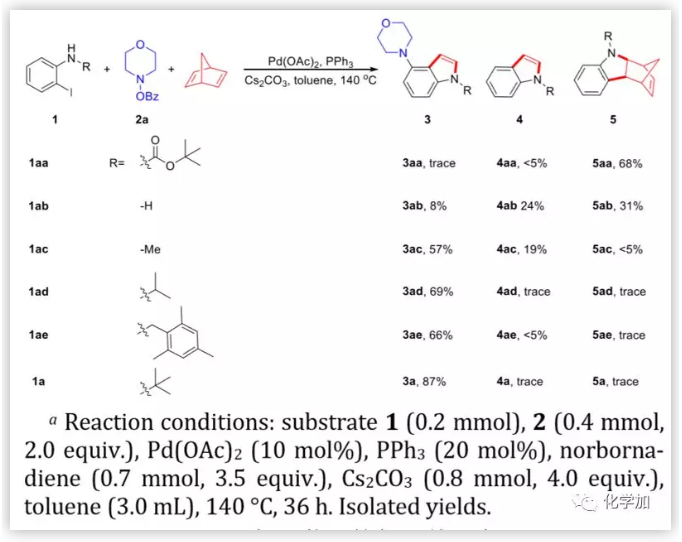
圖2. 鄰碘苯胺的保護基研究(圖片來源:J. Am. Chem. Soc.)
首先,作者采用可脫除的叔丁氧基羰基(Boc)作為鄰碘苯胺的保護基,用降冰片二烯(NBD)代替降冰片烯(NBE)作為Catellani反應的鄰位C-H胺化的暫時媒介,期望一步合成4-氨基吲哚骨架結構。不幸的是,沒有檢測到想要的產物,發生了分子內Buchwald偶聯,而沒有進行逆Diels-Alder反應。以未保護的鄰碘苯胺為底物,采用氣相色譜-質譜(GCMS)技術,作者發現生成了少量的目標產物。一些直接分子內的Buchwald偶聯產物5ab可通過逆Diels-Alder反應轉化為4ab。作者推測,氮原子上的給電子基團可以使反應朝著鄰位C-H胺基化方向反應,并促進逆Diels-Alder反應進行。因此,作者用N-甲基-鄰碘苯胺作為底物。令人驚喜的是,獲得了4-氨基吲哚產物3ac,產率為57%,幾乎所有的5ac都轉化為了4ac。隨后,作者進一步研究了異丙基和叔丁基作為保護基,空間位阻對反應方向的影響。當使用叔丁基時,以87%的產率獲得了4-氨基吲哚3a,GCMS未檢測到其他副產物。此外,多取代芐基(1ae)作為保護基時也可以順利得到目標產物。三苯基膦是該反應最好的配體。
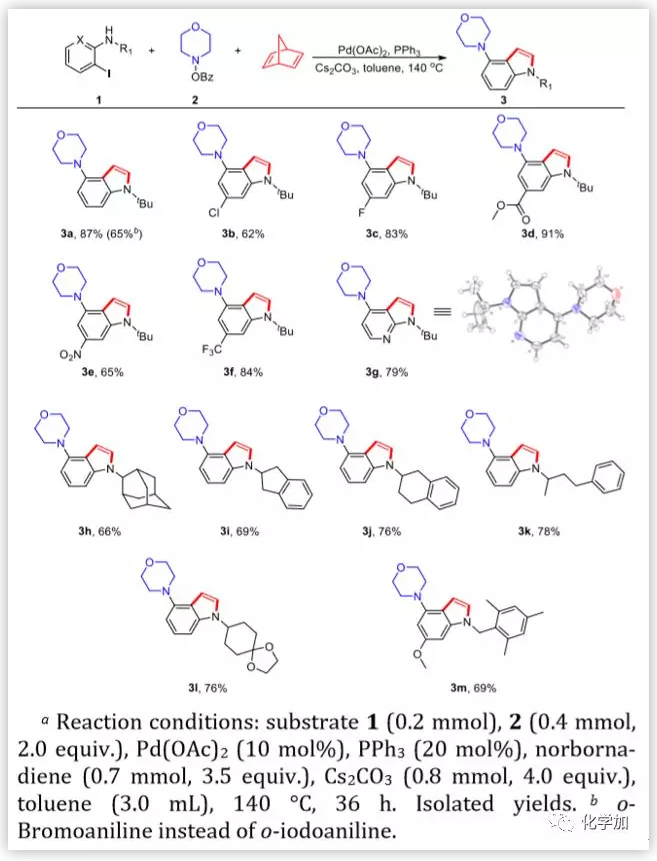
圖3. 底物范圍考察(圖片來源:J. Am. Chem. Soc.)
接著,作者對底物范圍進行了考察,首先研究了鄰碘苯胺的底物范圍。具有鹵素(-F,Cl)和強吸電子基(-NO2)的鄰碘苯胺與反應體系相兼容,并能以優異的收率得到所需的4-氨基吲哚產物(3b-3f)。值得一提的是,雜芳族底物3-碘吡啶-2-胺反應平穩,得到4-氨基-7-氮雜吲哚3g,收率79%。隨后,作者擴大了鄰碘苯胺氮原子上的基團范圍。具有大位阻的金剛烷3h、二氫茚3i、四氫萘3j和含有芳基烴4-苯基-2-丁基的3k都能以優良的收率獲得目標產物。這些實例表明,通過該反應可以合成一系列N-烷基取代的4-氨基吲哚。值得注意的是,吲哚與仲碳或叔碳的偶聯反應目前是一個難題,該方法為合成這些吲哚衍生物提供了方便的途徑。
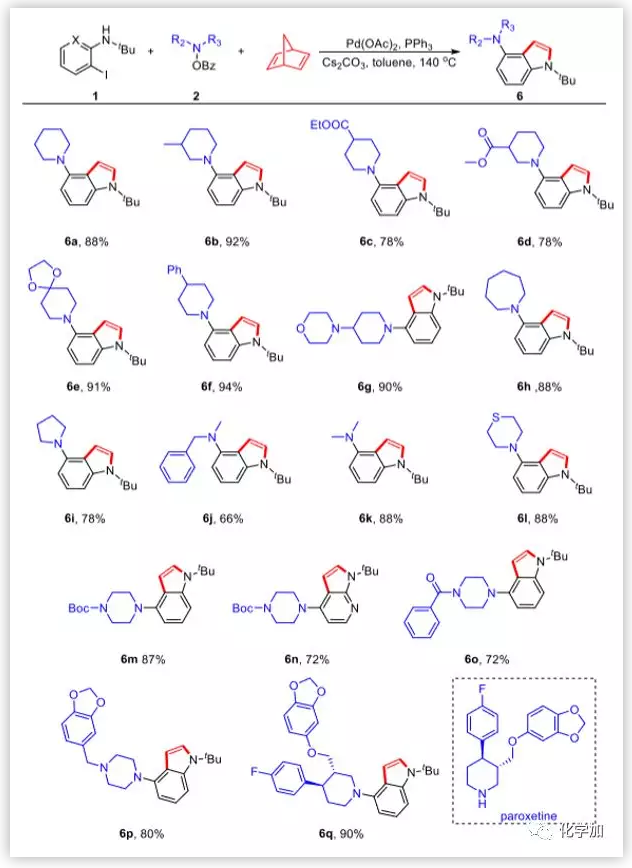
圖4. 親電胺化試劑的考察(圖片來源:J. Am. Chem. Soc.)
作者繼續擴大親電胺化試劑的范圍。不同取代基團的哌啶、硫代嗎啉和Boc-保護的哌嗪衍生的胺化試劑均以優異的產率得到所需產物。非六環胺化試劑,例如氮雜環庚烷、吡咯烷、二甲胺和甲基芐基氨,也以優良的產率得到目標產物,而之前工作中這類親電胺化試劑作為底物的產率非常低。特別地,抗抑郁藥帕羅西汀的吲哚衍生物可以通過該方法直接得到(6q)。
為進一步證明該方法的實用價值,作者擴大了親電試劑的范圍。使用溴代烷基和芳基作為親電試劑,并重新優化了反應條件。當使用N,N-二甲基甲酰胺代替甲苯作溶劑時,成功地得到4-烷基和芳基取代的吲哚。但該方法不能合成雜環吲哚衍生物。
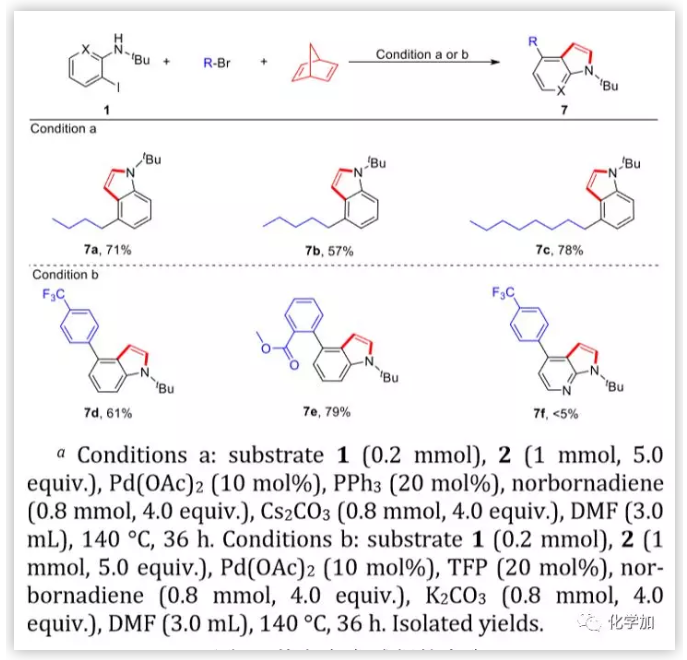
圖5. 其它親電試劑的考察(圖片來源:J. Am. Chem. Soc.)
為了證明該方法的工業化潛力,在4 mmol規模上進行反應,能以79%的產率得到目標產物。藥物化合物和天然產物通常含有未保護的N-H鍵,因此作者對4-氨基吲哚進行了脫保護實驗。當氯化鋁作Lewis酸并且在DCM中55 ℃下反應時,得到脫保護產物3ab,產率為76%。另外,作者還對吲哚3a進行了碘化和Friedel-Crafts三氟乙酰化。最后,根據Catellani的工作,作者嘗試使用二苯乙炔和降冰片烯代替降冰片二烯,但是僅產生了痕量的所需產物10。這可能是由于脫降冰片烯過程速率遠低于分子內Buchwald偶聯(圖6)。
在GPCR靶標的分子砌塊4-哌嗪吲哚的合成中進一步證明了該方法的實用性,作者還利用它進一步合成了用于治療胰腺導管腺癌的GOT1抑制劑。以前的方法非常不經濟且對環境不友好,合成4-哌嗪吲哚需要3-5步且產率極低。通過新策略,作者通過一步三組分串聯反應和簡單的脫保護過程合成了4-哌嗪基吲哚。然后,在三乙胺存在下,將4-哌嗪吲哚和4-氯苯基異氰酸酯攪拌30分鐘,得到GOT1抑制劑,收率46%。
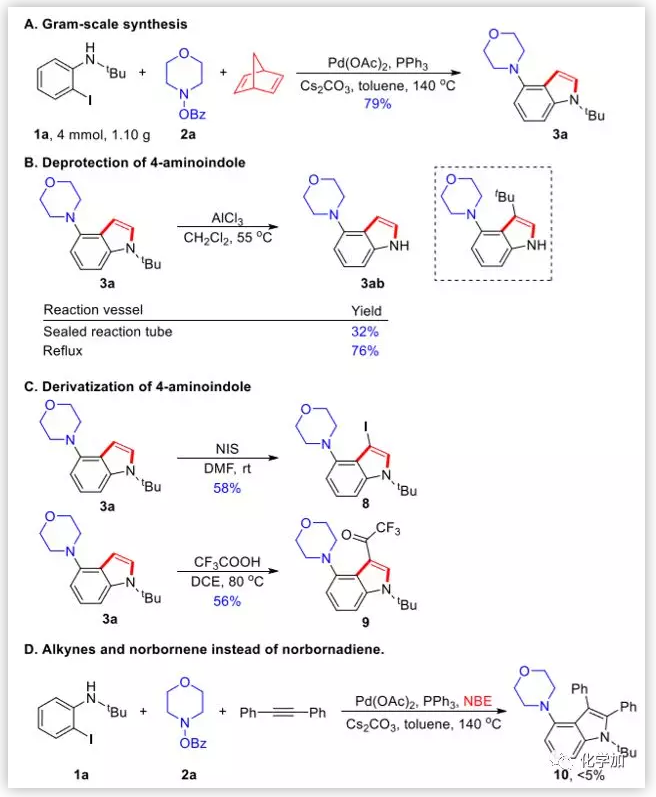
圖6. 產物的衍生化(圖片來源:J. Am. Chem. Soc.)
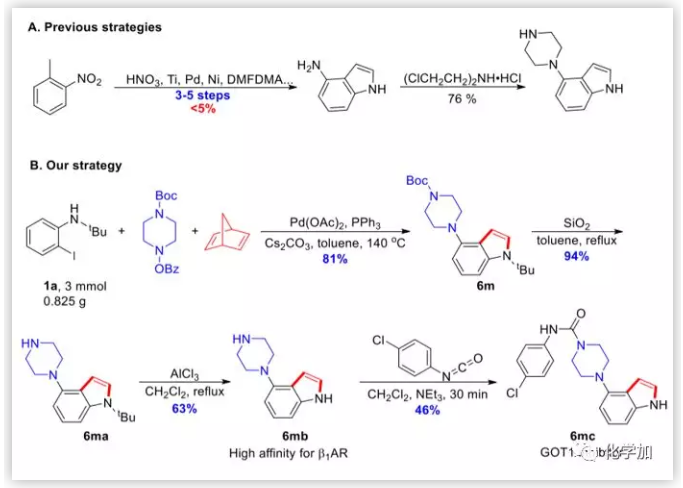
圖7. 在藥物合成中的應用(圖片來源:J. Am. Chem. Soc.)
作者還通過DFT計算研究了帶有不同保護基(Boc,t-Bu)的鄰碘苯胺的反應機理。在整個機理研究中考慮了Cs2CO3的作用。在C-H活化之前,對于t-Bu中間體A,脫去CsI釋放3.2 kcal/mol能量,形成B1;對于Boc中間體F,脫去CsI釋放2.4 kcal/mol能量,形成G1。對于C-H活化過程,能壘分別為25.3和24.5 kcal/mol。可以旋轉中間體B1和G1的苯環以獲得中間體B2和G2。值得注意的是,由于叔丁基的大位阻,B2的能量比B1的能量大0.6 kcal/mol。這是當保護基為叔丁基時反應向鄰位C-H活化方向進行的原因之一。
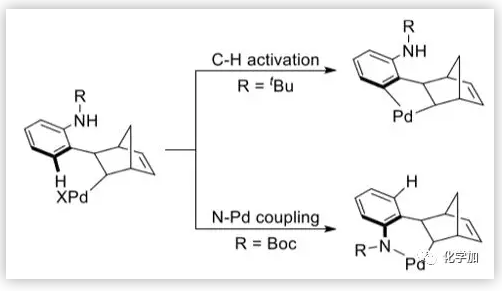
圖8. C-H活化和Buchwald偶聯(圖片來源:J. Am. Chem. Soc.)
隨后,作者研究了分子內C(sp3)-N Buchwald偶聯的機理。對于中間體B2,碳酸根中的氧與叔丁基中的氫之間的距離為2.35 ?。因此,碳酸根和叔丁基之間的空間位阻阻止了Pd直接被氮原子進攻。根據碳酸根和胺之間的氫鍵以及Buchwald配體和鈀的配位模式,作者推測苯與鈀的配位可能導致碳酸根的羰基離去。結果是,碳酸鹽可以通過16.1 kcal/mol的能壘從胺中除去質子,苯環可以與鈀配位形成中間體D。然后發生1,3-Pd遷移獲得中間體E。鄰位胺化后,Buchwald偶聯過程的能壘明顯減小。
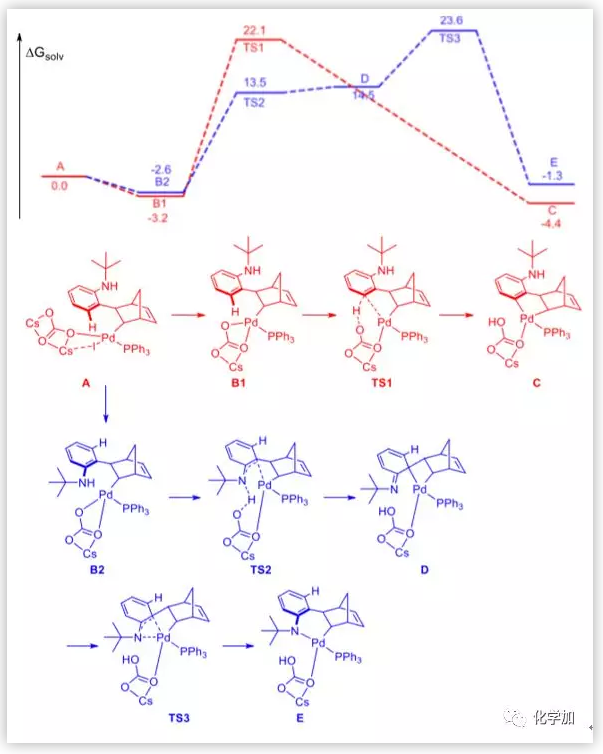
圖9. DFT計算的吉布斯自由能圖(叔丁基)(圖片來源:J. Am. Chem. Soc.)
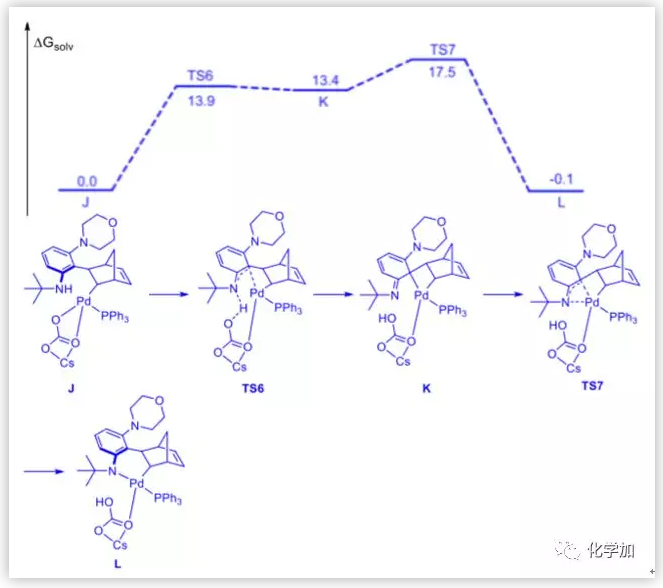
圖10. 鄰位胺化后的吉布斯自由能圖(圖片來源:J. Am. Chem. Soc.)
當保護基是Boc時,作者以相同的方式計算。但是沒有形成類似于中間體D的去芳構化中間體。相反,直接形成中間體I。這可能是由于Boc和碳酸根之間的空間位阻很小。因此,作者推測這個過程是一個協同的金屬化過程,然后找到了TS5。
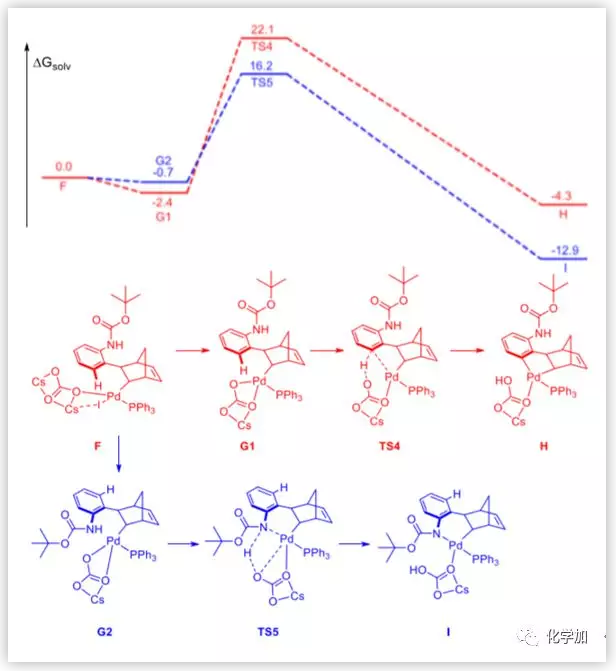
圖11. DFT計算的吉布斯自由能圖(Boc)(圖片來源:J. Am. Chem. Soc.)
簡而言之,當保護基是叔丁基時,Buchwald偶聯的能壘比C-H活化的能壘大0.9 kcal/mol。當保護基是Boc時,Buchwald偶聯的能量比C-H活化的能量低7.6 kcal/mol。計算結果與實驗結果一致。
總結:通過Catellani和逆Diels-Alder策略,從鄰碘苯胺、N-苯甲酰氧基胺和降冰片二烯出發,經三組分交叉偶聯合成了高度官能化的4-氨基吲哚。基于DFT計算,該反應的分子內Buchwald偶聯經歷了去芳構化和1,3-鈀遷移過程。反應條件溫和、底物適用性廣泛,還可以用于4-哌嗪基吲哚和GOT1抑制劑的合成。該方法在吲哚類生物堿和含4-氨基吲哚的藥物分子合成中具有重要應用價值。該研究得到國家自然科學基金的大力支持,相關成果發表在Journal of the American Chemical Society 上。蘭州大學的張博生博士和香港中文大學的李宇科博士是該論文的共同第一作者,梁永民教授為本文的通訊作者。
撰稿人:詩路化語
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn