



芳基腈是一類重要的化合物,其是藥物,農(nóng)用化學(xué)品和天然產(chǎn)物中重要的結(jié)構(gòu)單元。此外,氰基官能團(tuán)也可以容易地衍生成各種重要官能團(tuán),如羧基衍生物、醛、胺和雜環(huán)。目前,過(guò)渡金屬催化的直接C-H鍵氰化反應(yīng)是合成芳香族氰化物的有效方法(圖1c)。盡管C-H鍵氰化已取得重大進(jìn)展,但是其苛刻的反應(yīng)條件(加熱超過(guò)100 ℃)和不可回收的反應(yīng)體系限制了其實(shí)際應(yīng)用。因此,發(fā)展溫和高效可回收的氰化策略仍然是必要的。
近年來(lái),離子液體(ILs)在有機(jī)合成中已被廣泛用作穩(wěn)定且可回收的反應(yīng)介質(zhì)和催化劑。與傳統(tǒng)的有機(jī)試劑相比,離子液體具有熔點(diǎn)低、毒性低、電導(dǎo)率高、化學(xué)穩(wěn)定性好、熱穩(wěn)定性好、溶解性好、易于回收利用等獨(dú)特的優(yōu)點(diǎn)。迄今為止,離子液體已成功應(yīng)用于Suzuki反應(yīng)、Heck 反應(yīng)、Michael加成,Diels-Alder環(huán)加成反應(yīng)和立體選擇性鹵化反應(yīng)等,然而,它們?cè)贑-H活化氰化中的應(yīng)用尚未見(jiàn)報(bào)道。

(圖1 芳基腈的合成策略)
研究初期,作者以2-苯基吡啶1a與N-氰基-N-苯基-對(duì)甲苯磺酰胺(NCTS,2)為模型底物,考察了Rh催化C-H鍵氰化的可行性(圖 2)。當(dāng)1-丁基-3-甲基咪唑雙(三氟甲磺酰基)酰亞胺([BMIM] NTf2)作為反應(yīng)介質(zhì)時(shí),反應(yīng)能以58%的收率得到目標(biāo)鄰氰化物產(chǎn)物3a(Table 1, entry 1)。隨后,為優(yōu)化3a的收率,作者對(duì)反應(yīng)條件進(jìn)行篩選,發(fā)現(xiàn)[Cp*RhCl2]2比其它Rh(Ⅲ)催化劑具有更好的催化活性(entries 14)。接著,作者對(duì)離子液體中陰、陽(yáng)離子的組合進(jìn)行了探索。值得注意的是,只有含咪唑鎓作為陽(yáng)離子的離子液體對(duì)反應(yīng)有效,且[BMIM]NTf2最佳。此外,將反應(yīng)時(shí)間延長(zhǎng)至48小時(shí),增加NCTS和銀鹽的當(dāng)量使收率提高至78%。
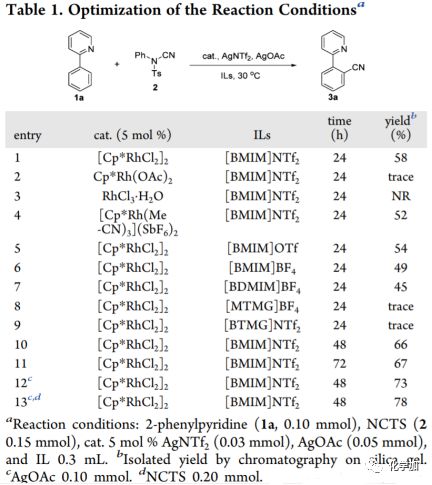
(圖 2 條件優(yōu)化)
在最優(yōu)反應(yīng)條件下,作者首先考察了2-苯基吡啶的C-H鍵氰化。連有給電子基或吸電子基的底物都能與反應(yīng)體系兼容,并以良好的收率得到相應(yīng)的氰化產(chǎn)物3a-3l。當(dāng)2-苯基部分被2-聯(lián)苯基,2-萘基和2-噻吩基取代時(shí),與3a相比,3m-3o的收率明顯提升。有趣的是,當(dāng)2-芳香環(huán)被2-脂肪族環(huán)取代時(shí)(如2-環(huán)己烯),氰化反應(yīng)仍能繼續(xù)進(jìn)行形成產(chǎn)物3p,收率為73%。該結(jié)果表明氰化反應(yīng)不僅能直接芳族官能化,也可以應(yīng)用于脂族烯烴。值得注意的是,將導(dǎo)向基團(tuán)(DG)變?yōu)槠渌鸑-雜環(huán)如嘧啶,吡唑和三唑也能順利得到氰化產(chǎn)物3q3v。
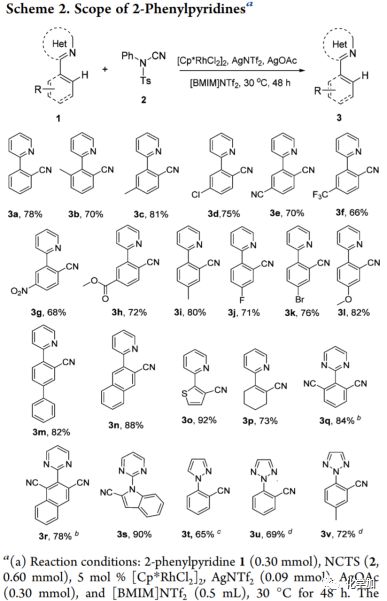
(圖3 2-苯基吡啶的底物范圍)
在上述成果的鼓舞下,作者繼續(xù)考察在氰化反應(yīng)中利用肟作導(dǎo)向基的可行性。幸運(yùn)的是,1-苯基-O-甲基肟可以80%的分離產(chǎn)率得到5a。各種常見(jiàn)的官能團(tuán)(如甲基,甲氧基,鹵素,甚至硝基)都具有良好的耐受性,并以良好至優(yōu)異的收率得到相應(yīng)的產(chǎn)物5b5k。肟醚的空間位阻使得5n和5o的收率有所降低,并且未觀察到產(chǎn)物5p。
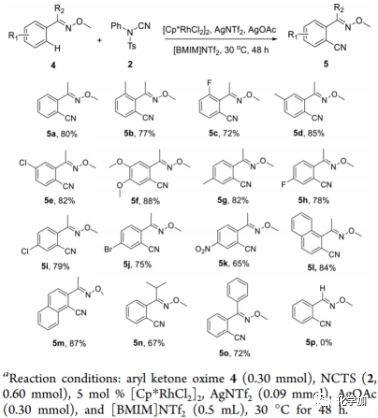
(圖4 芳基酮肟醚的底物范圍)
為了闡明該反應(yīng)的機(jī)理,作者進(jìn)行了一系列實(shí)驗(yàn)。H/D交換實(shí)驗(yàn)經(jīng)1H NMR譜監(jiān)測(cè)到1a中40%的鄰位C-H鍵被氘化,這表明C-H活化是可逆的。1c和1f的分子間競(jìng)爭(zhēng)實(shí)驗(yàn)表明C-H鍵氰化反應(yīng)有利于富電子底物。在相同條件下,作者利用1a和d5-1a與偶聯(lián)劑NCTS(2)進(jìn)行反應(yīng),測(cè)得其動(dòng)力學(xué)同位素效應(yīng)值kH/kD為2.8,這表明C-H鍵斷裂是反應(yīng)的決速步。
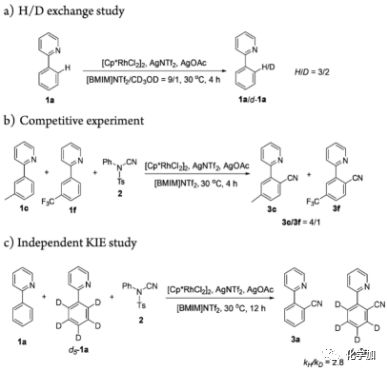
(圖5 機(jī)理實(shí)驗(yàn))
基于上述結(jié)果和以往的相關(guān)報(bào)道,作者提出了一個(gè)可能的反應(yīng)機(jī)制。首先,用AgOAc處理Rh前體產(chǎn)生反應(yīng)性陽(yáng)離子Rh物種A,其與2-苯基吡啶1a反應(yīng),得到具有空位配位位點(diǎn)的環(huán)狀Rh物種B。B與2反應(yīng)形成緊密過(guò)渡態(tài)C,其也是反應(yīng)的關(guān)鍵中間體。然后,過(guò)渡態(tài)C經(jīng)消除形成產(chǎn)物3a和銠絡(luò)合物D。最后,在質(zhì)子存在下,得到活性Rh物種A并參與下一個(gè)催化循環(huán)。

(圖 6 可能的機(jī)理)
重要的是,芳香族氰化物作為藥物設(shè)計(jì)的合成砌塊具有重要意義。例如,上市藥物SuvxEnter是一種新型食欲素拮抗劑,且已成為治療原發(fā)性失眠癥的一類新型藥物。作者利用5-甲基-2-(2H-1,2,3-三唑-2-基)-芐腈(產(chǎn)物3u)經(jīng)兩步合成Suvorexant,產(chǎn)率為79%。該成果可能為藥物的設(shè)計(jì)和合成提供新思路。
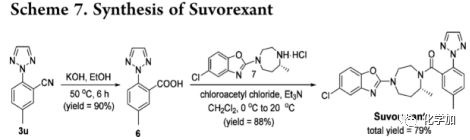
(圖7 合成Suvorexant)
總結(jié):吳勇教授課題組實(shí)現(xiàn)了利用離子液體[BMIM]NTf2作為可回收介質(zhì)的首例C-H鍵氰化策略。該方法擴(kuò)展了Rh催化C-H官能化反應(yīng)的應(yīng)用范圍,即首次在室溫下以可回收的方式實(shí)現(xiàn)了氰化反應(yīng)。此外,在該方法中可以使用多種不同的導(dǎo)向基團(tuán),并成功合成了許多芳族和雜芳腈。
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn