




第一作者:Hanyu Liang(梁撼宇)
通信作者:Xiao Xiao(肖曉), Baoguo Zhao?(趙寶國)
通訊單位:上海師范大學(xué),上海交通大學(xué)
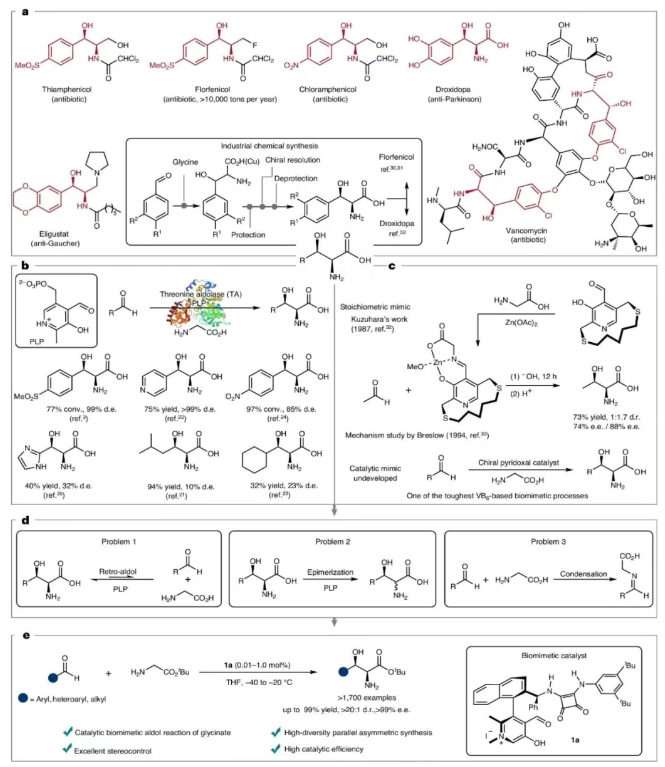
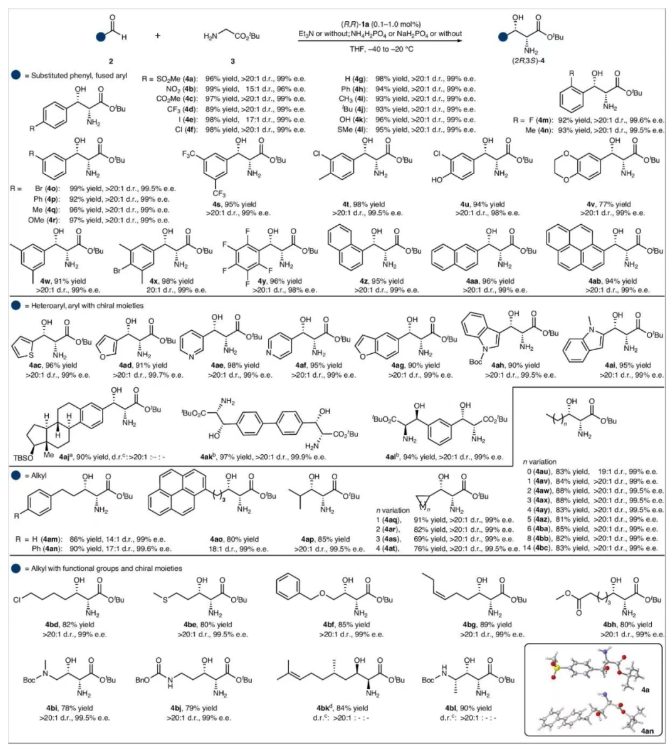
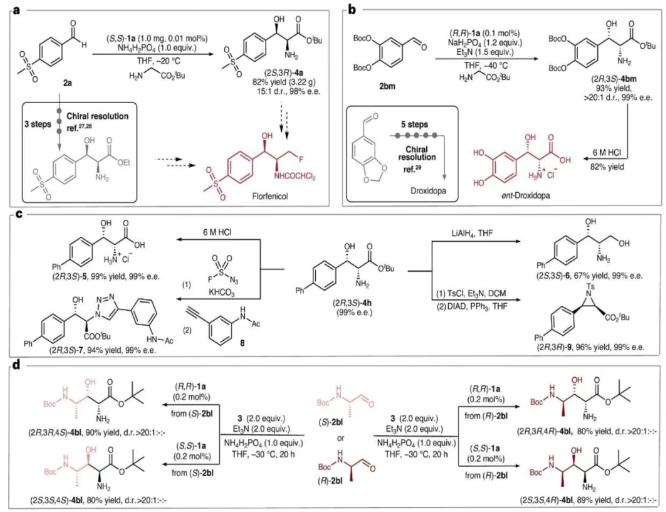
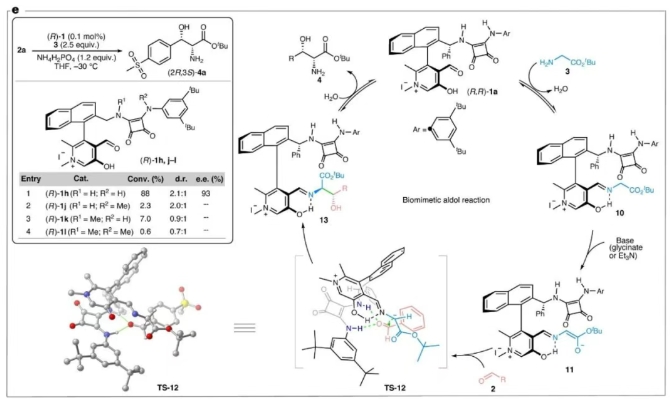
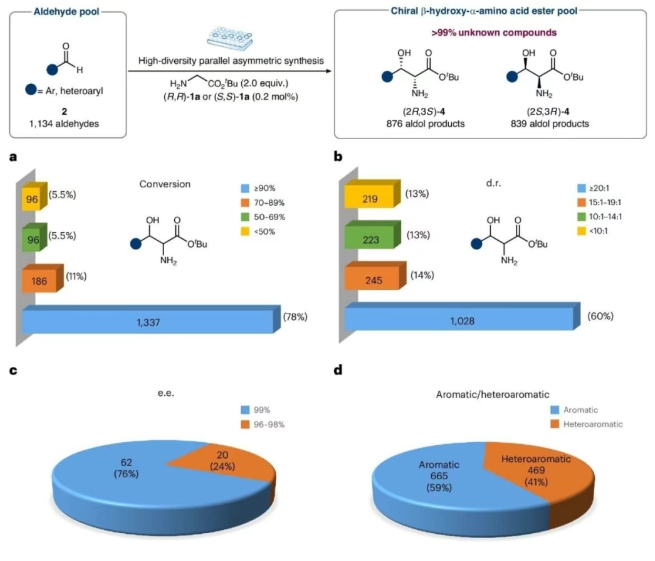
導(dǎo)讀 正文 蘇氨酸醛縮酶催化合成手性β-羥基-α-氨基酸面臨底物范圍受限和β-碳立體選擇性不足的雙重瓶頸(圖1b)。該生物過程的仿生模擬始終未能突破計量模擬的局限(圖1c)。仿生aldol反應(yīng)為手性β-羥基-α-氨基酸的高效合成提供了新思路,但面臨多重挑戰(zhàn):反應(yīng)的可逆性導(dǎo)致產(chǎn)物易發(fā)生分解;產(chǎn)物在吡哆醛催化條件下傾向于發(fā)生差向異構(gòu)化;醛與甘氨酸形成的亞胺會顯著抑制aldol反應(yīng)(圖1d)。作者發(fā)展了方酰胺側(cè)鏈修飾的手性吡哆醛催化劑,整合了多重活化、協(xié)同催化和底物識別等生物催化特征,它是實現(xiàn)甘氨酸酯仿生不對稱aldol反應(yīng)的關(guān)鍵(圖1e)。 圖1. 手性β-羥基-α-氨基酸及其合成方法 作者成功實現(xiàn)了甘氨酸酯仿生aldol反應(yīng)。該轉(zhuǎn)化具有優(yōu)秀的底物適應(yīng)性:取代芳基醛、雜芳醛和烷基醛均能順利反應(yīng),以高產(chǎn)率、優(yōu)秀立體選擇性(up to >20:1 dr和 >99% ee)生成一系列手性β-羥基-α-氨基酸酯。醛的電子性質(zhì)對反應(yīng)影響較小,富電子與缺電子底物均具較高活性。該反應(yīng)具有重要的應(yīng)用價值:抗生素類藥物(甲砜霉素、氟苯尼考、氯霉素、萬古霉素)、代謝調(diào)節(jié)藥物(伊利格魯司)、天然產(chǎn)物(乳胞素、二氫鞘氨醇)以及多種生物活性分子(4h、4af、4at等)的關(guān)鍵結(jié)構(gòu)均可通過該反應(yīng)高效合成(圖2)。 圖2. 甘氨酸酯與醛的不對稱aldol反應(yīng)的底物拓展情況 該反應(yīng)可用于多種藥物的快速構(gòu)建:在0.01 mol%的催化劑用量下,一步立體選擇性構(gòu)建氟苯尼考關(guān)鍵中間體L-蘇-對甲磺酰苯丙氨酸酯(82% yield、15:1 dr和98% ee)(圖3a);藥物分子屈昔多巴也可以通過仿生aldol反應(yīng)兩步快速合成(圖3b)。同傳統(tǒng)合成方法相比,仿生合成路線無需手性拆分,避免了復(fù)雜的保護基操作,顯著縮短了合成步驟,具備明顯的成本和環(huán)境優(yōu)勢。手性β-羥基-α-氨基酸酯產(chǎn)物具有重要的合成價值,可作為多功能合成子靈活轉(zhuǎn)化為各類關(guān)鍵手性化合物(圖3c)。此外,以手性醛2bl為起始原料,該反應(yīng)還能實現(xiàn)立體發(fā)散性合成,高效制備四種非對映異構(gòu)體(圖3d)。 圖3.合成應(yīng)用及產(chǎn)物衍生化 反應(yīng)遵循與酶促aldol反應(yīng)類似的機理:吡哆醛1a通過與甘氨酸酯形成亞胺10,活化其α-C–H鍵,去質(zhì)子化形成離域碳負離子11,對醛3進行不對稱加成并水解,釋放出產(chǎn)物β-羥基-α-氨基酸酯4,并再生催化劑1a。該反應(yīng)展現(xiàn)出的高活性和優(yōu)異選擇性源于催化劑獨特的結(jié)構(gòu):吡哆醛片段通過共價作用高效活化甘氨酸酯;方酰胺側(cè)鏈借助雙重氫鍵網(wǎng)絡(luò)精確活化醛基底物;聯(lián)芳基骨架與側(cè)鏈協(xié)同構(gòu)建的手性空腔實現(xiàn)了對醛類底物的立體專一性識別。這種多機制協(xié)同的催化作用,包括共價活化、氫鍵協(xié)同作用以及立體選擇性識別,共同構(gòu)成了其卓越催化性能的結(jié)構(gòu)基礎(chǔ)(圖4)。 圖4. 機理研究 該反應(yīng)具有罕見的高效性和廣譜性,運用高通量合成策略,可以快速構(gòu)建數(shù)以萬計的手性β-羥基-α-氨基酸酯。為了展示該反應(yīng)在構(gòu)建分子結(jié)構(gòu)多樣性方面的強大能力,作者通過高通量手性合成技術(shù),成功構(gòu)建了一個包含1700多種手性β-羥基-α-氨基酸酯的高活性化合物庫,為后續(xù)的藥物篩選提供了物質(zhì)基礎(chǔ)。盡管底物結(jié)構(gòu)高度多樣,大多數(shù)反應(yīng)仍具有優(yōu)秀的轉(zhuǎn)化率和立體選擇性。反應(yīng)無需分離純化,經(jīng)簡單后處理即可得到較高純度的目標產(chǎn)物,特別適用于以快速篩選為目的生物活性研究(圖5)。 總結(jié) 綜上所述,趙寶國教授和肖曉教授團隊以0.01-1 mol%手性吡哆醛為催化劑,實現(xiàn)了甘氨酸酯的仿生aldol反應(yīng),為手性β-羥基-α-氨基酸提供了高效的通用合成方法,并能快速構(gòu)建結(jié)構(gòu)多樣的高活性分子庫,對新藥研發(fā)和藥物高效合成都有重要意義。該仿生反應(yīng)通過簡單分子的一鍵鏈接實現(xiàn)了重要功能分子的高效構(gòu)建,具有極高的效率、極廣的底物適應(yīng)性和多維選擇性的精準控制,是一個適應(yīng)藥物化學(xué)、AI與高通量合成等新發(fā)展要求的理想反應(yīng)新范例。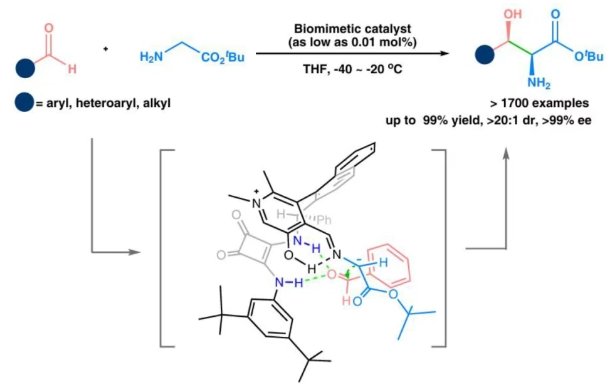
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn