



(圖片來源:Science)
正文
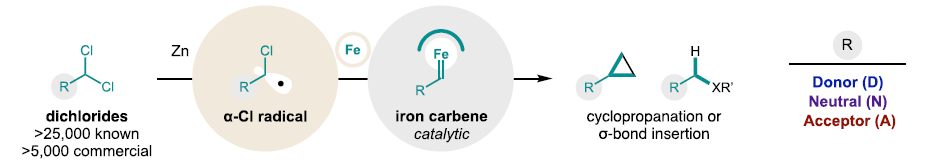
金屬卡賓作為有機合成中極具價值的高活性中間體,其催化合成仍面臨兩大挑戰(zhàn):1)并非所有極性類型的卡賓都能通過催化途徑獲得;2)缺乏能制備全系列電子特性卡賓的通用前體。最近,美國俄亥俄州立大學David A. Nagib課題組突破性地開發(fā)了鐵催化的反應策略,其可合成包含供電子(OMe、NR2、烷基)、吸電子(CN、CO2R)及電中性(H、BR2、SiR3、鹵素、芳基/雜芳基)取代的卡賓。該策略通過α-氯自由基途徑,實現(xiàn)了(2+1)環(huán)丙烷化和σ鍵插入反應的廣譜卡賓偶聯(lián)。這一溫和、高效且電子特性可調的合成方法,不僅建立了基于動力學和熱力學參數(shù)的金屬卡賓分類新標準,還衍生出類似于點擊化學的卡賓反應及其水相適配的反應體系,為化學生物學應用提供了新工具(Fig. 1)。歡迎下載化學加APP到手機桌面,合成化學產業(yè)資源聚合服務平臺。
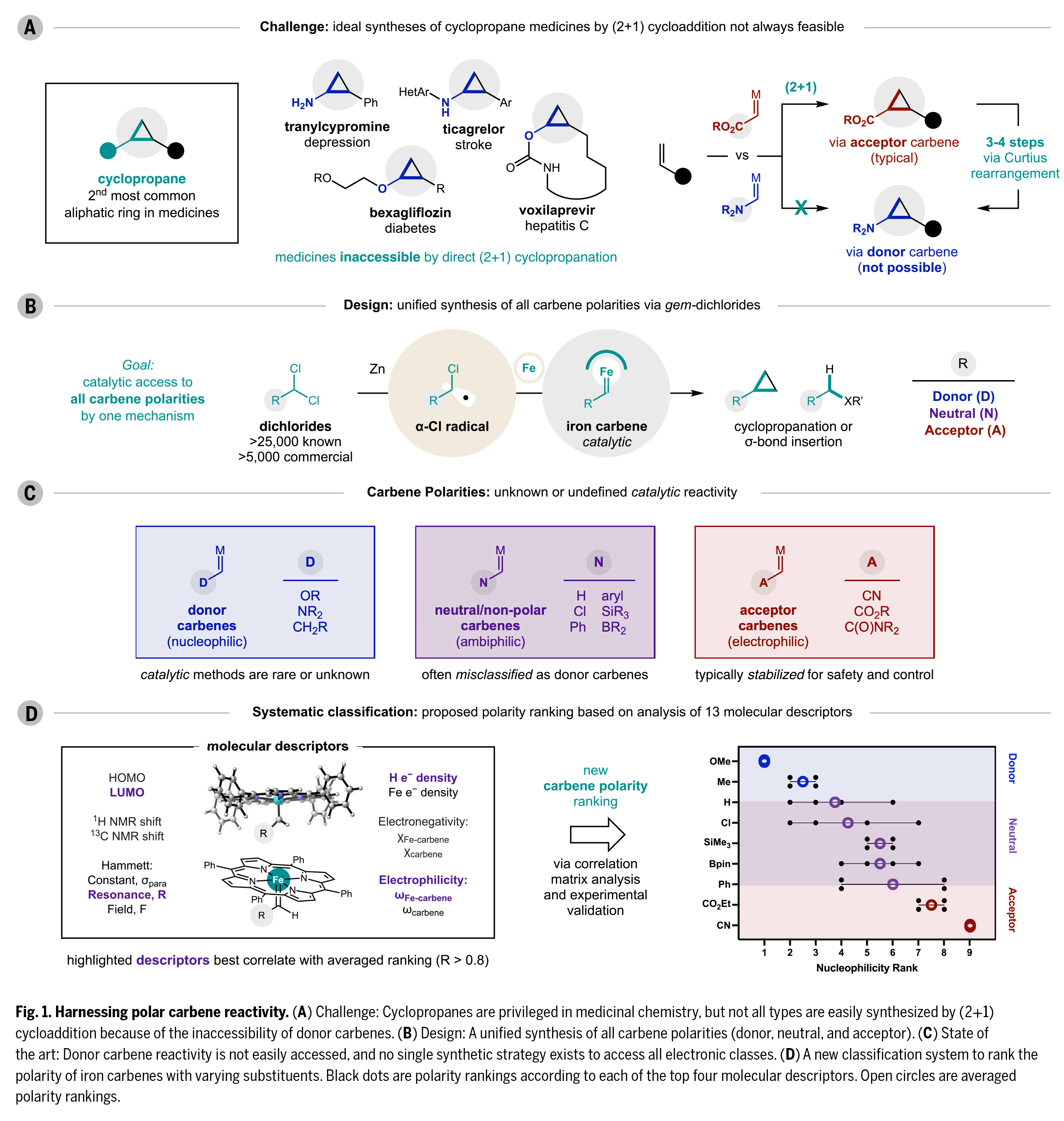
(圖片來源:Science)
首先,作者成功開發(fā)了一種基于商業(yè)可得的偕二氯化合物與烯烴的(2+1)環(huán)丙烷化反應(FeTPPCl為預催化劑,Zn為還原劑,LiI為自由基介導物)(Fig. 2A)。該策略適用于多種極性卡賓,包括供電子卡賓(R = OMe或NR2,1-3,65-96%)、烷基卡賓(4,93%)、CH2Cl2/CD2Cl2前體產生的卡賓(R = H/D,5-6,99%)以及偕二烷基卡賓(7,41%)。特別值得注意的是,中性鐵卡賓可通過鹵仿(8-10,70-82%)、硅基/硼基二氯化合物(11-12,70-90%)等前體制備,且所得的連有鹵素、硼酸酯等官能團的環(huán)丙烷產物可進一步官能團化。此外,芳基卡賓(13-16,75-93%)和連有吸電子基團修飾的卡賓(酯基17,85%、氰基18,99%)也表現(xiàn)優(yōu)異。
此外,該反應對烯烴底物同樣展現(xiàn)出廣譜適用性(Fig. 2B)。其中,1,1-二取代脂肪族烯烴與苯乙烯類似物可高效反應,環(huán)外烯烴可構建含氮雜環(huán)丁烷、環(huán)丁烷等藥用常見結構的螺環(huán)產物(19-20,95%)。烯酰胺(21,60%)、乙烯基鄰苯二甲酰亞胺(22,81%)和烯醇醚(23,70%)等雜原子烯烴也可順利轉化,立體選擇性優(yōu)異(dr > 10:1)。以硼酸酯修飾的環(huán)丙烷24為例,其可通過氧化、格氏加成、交叉偶聯(lián)等反應衍生為醇25(73%)、烯烴26(56%)和芳烴27(98%),且完全保持立體構型。
值得注意的是,該反應在酮、酯、醇、硫醚等添加劑存在下仍能保持> 50%的產率(35),展現(xiàn)出優(yōu)異的官能團兼容性(Fig. 2C)。三級胺可完全兼容,而伯/仲胺、酰胺和醛類則會發(fā)生副反應。這一模塊化策略為復雜分子中環(huán)丙烷結構的構建提供了高效途徑。
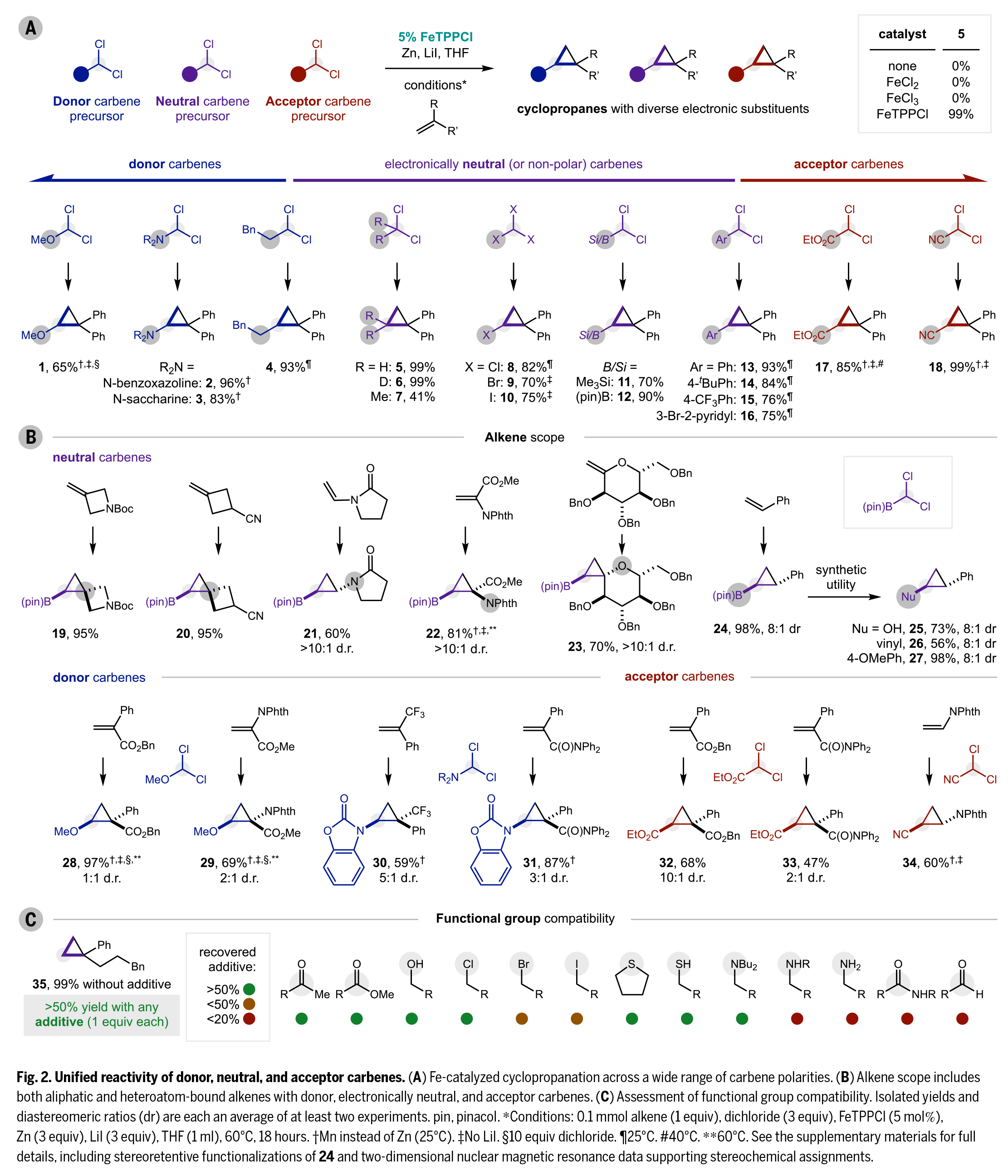
(圖片來源:Science)
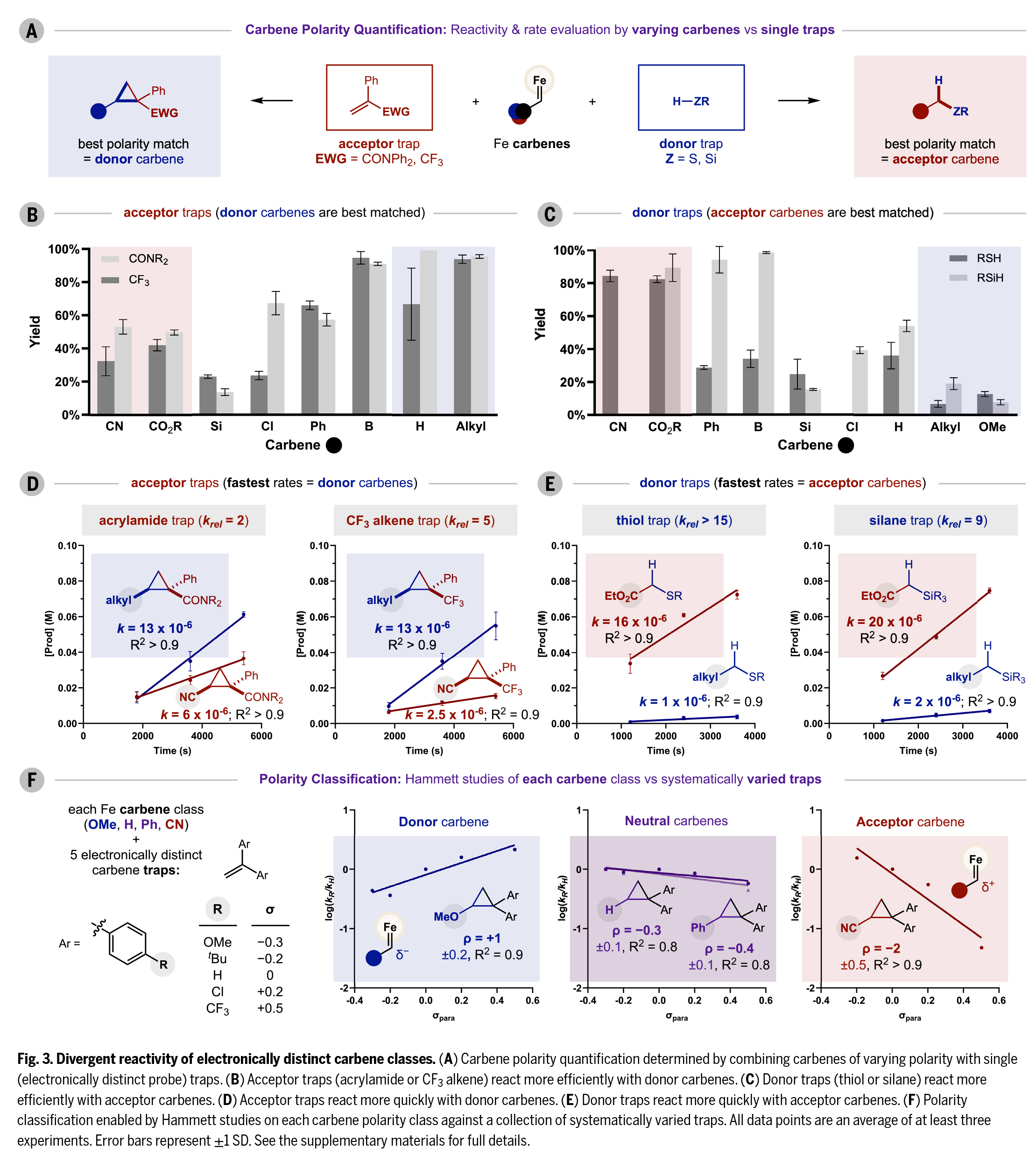
接下來,作者通過三種策略系統(tǒng)研究了卡賓極性對反應活性的影響機制(Fig. 3)。首先,針對九類代表性R基團,分別選用兩種缺電子受體捕獲劑(丙烯酰胺和三氟甲基烯烴,Fig. 3A紅色)和兩種富電子供體捕獲劑(硫醇和硅烷,Fig. 3A藍色)進行平行實驗。標準條件下16小時的實驗數(shù)據(jù)顯示(Fig. 3B):供體卡賓與受體捕獲劑反應活性最高(產率顯著高于中性/受體卡賓),而受體卡賓則與供體捕獲劑反應更優(yōu)(Fig. 3C),中性卡賓介于兩者之間。動力學研究表明(Fig. 3D-E),供體(烷基)卡賓與受體捕獲劑的反應初速度是受體(氰基)卡賓的5倍;而受體(酯基)卡賓與供體捕獲劑的反應速度則比供體卡賓快10倍以上,這解釋了受體卡賓在σ鍵插入反應中的優(yōu)勢。
作者進一步通過四組Hammett研究定量表征卡賓極性(Fig. 3F):以對位取代苯乙烯為底物,測得供體(OMe)、中性(H)和受體(CN)卡賓的反應常數(shù)ρ分別為+1±0.2、-0.3±0.1和-2±0.5,準確反映了其電子特性。值得注意的是,芳基卡賓(Ph)實際表現(xiàn)為中性電性(ρ = -0.4±0.1),比CH2卡賓更具親電性,這與以往"供體卡賓"的認知不同。
(圖片來源:Science)
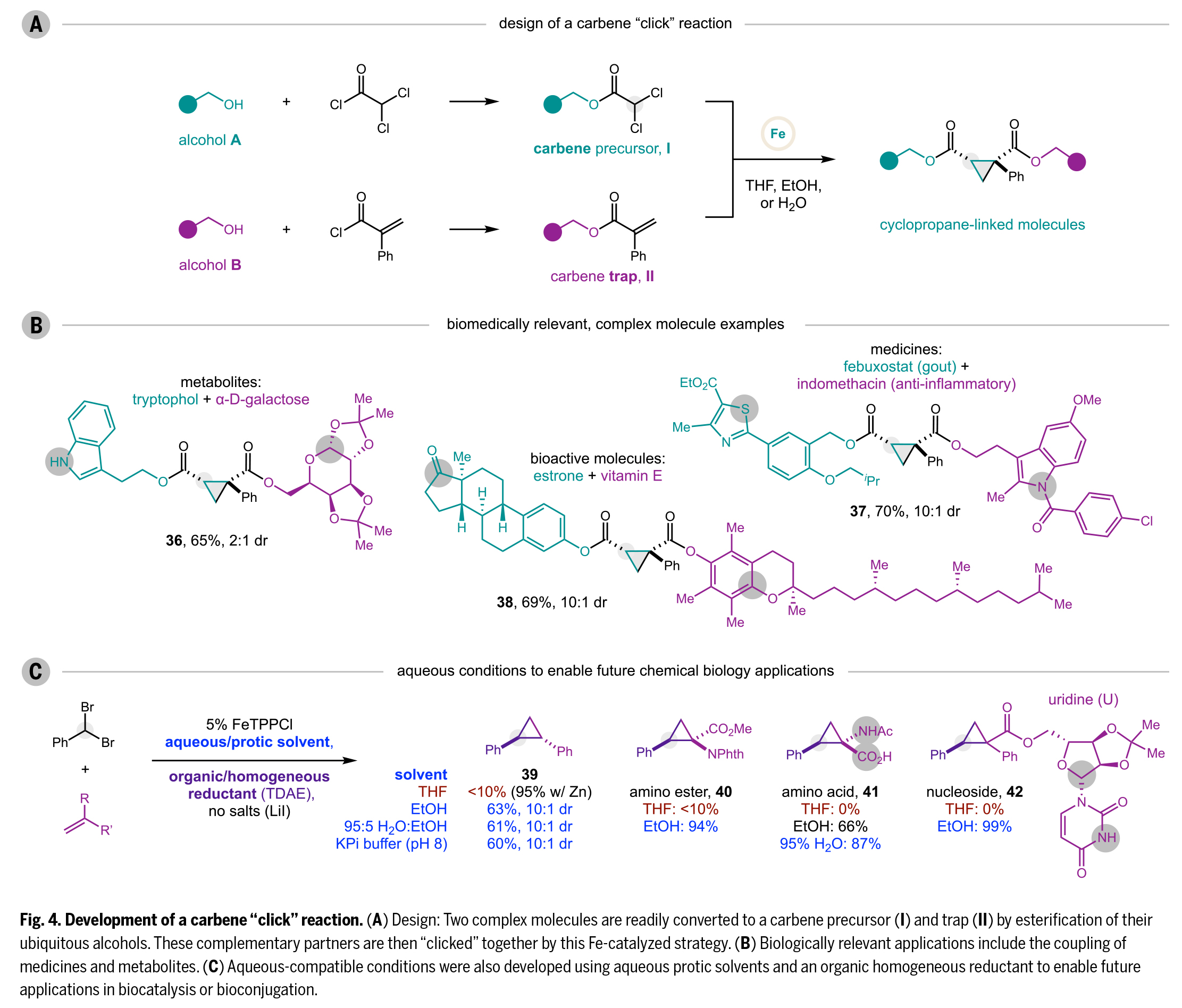
基于該方法的簡便性,作者開發(fā)了一種類點擊化學的卡賓偶聯(lián)反應(Fig. 4A),其高效性、選擇性和實用性可媲美(3+2)Huisgen環(huán)加成反應。與炔-疊氮環(huán)加成產生的三唑環(huán)相比,(2+1)環(huán)丙烷化能構建更小、更強且具有獨特空間取向的全碳環(huán),這些特性使其在藥物設計中備受青睞。該策略的創(chuàng)新之處在于:通過簡單的酰化將生物分子中的羥基轉化為互補反應模塊。醇A經α,α-二氯酰氯修飾形成卡賓前體I,醇B經α-苯基丙烯酰氯修飾形成卡賓捕獲劑II。如Fig. 4B所示,該方法成功實現(xiàn)了多種生物分子的高效偶聯(lián),包括代謝物(色氨醇與α-D-半乳糖,36,65%)、藥物(非布索坦與吲哚美辛,37,70%)和生物活性分子(雌酮與維生素E,38,69%)。其中灰色圓圈標示了傳統(tǒng)生物偶聯(lián)技術難以兼容的官能團,為重氮環(huán)丙烷方法提供了新的選擇。
針對水相體系的應用需求(如生物催化、生物偶聯(lián)或DNA編碼庫合成),作者進一步優(yōu)化了反應條件(Fig. 4C):(1)以有機還原劑TDAE(四(二甲氨基)乙烯)替代無機還原劑(Zn/Mn);(2)去除LiI鹽;(3)采用活性更高的偕二溴化物。該體系在乙醇中的反應效率優(yōu)于THF,且適用于含5%乙醇的緩沖水溶液(95:5 H2O:EtOH,KPi緩沖液pH 8)。除苯基卡賓與苯乙烯的模板反應(39)外,氨基酯40(94%)、氨基酸41(87%)和核苷42(99%)等質子性生物分子在質子溶劑中也表現(xiàn)出更佳的環(huán)丙烷化效率,這可能歸因于其溶解度的改善。
(圖片來源:Science)
總結
David A. Nagib課題組開發(fā)了一種基于商業(yè)可得試劑的通用催化策略,可通過統(tǒng)一機制調控各類卡賓極性。首次實現(xiàn)了全極性卡賓的催化統(tǒng)一合成,解決了供體卡賓難以直接生成的難題。通過實驗與計算結合,建立了卡賓極性的定量分類標準。為藥物設計(尤其是含環(huán)丙烷結構)提供了高效工具,將推動生物偶聯(lián)與材料化學發(fā)展。
聲明:化學加刊發(fā)或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn